Los mecanismos de acción por los cuales las bacterias ejercen su potencial psicobiótico no han sido completamente dilucidados. Sin embargo, se ha encontrado que estas bacterias brindan sus beneficios a través del sistema nervioso entérico o la estimulación del sistema inmunológico. Además, afectan al sistema nervioso o a la estimulación del sistema inmunitario. Además, afectan a los marcadores psicofisiológicos de depresión y ansiedad. Esto puede ocurrir de tres formas:
- Afectando la respuesta al estrés del eje hipotálamo-pituitario-suprarrenal (HPA) y reducir la inflamación sistémica
- Por un efecto directo sobre el sistema inmunitario
- Por la secreción de moléculas como neurotransmisores, proteínas y cadenas cortas de ácidos grasos.

Eje Hipotálamo-Pituitaria-Suprarrenal(Adrenal)
El eje HPA es el principal sistema de respuesta neuroendocrina para el estrés fisiológico y físico en el cuerpo humano. Incluye el hipotálamo, la glándula pituitaria y la corteza suprarrenal, así como algunos insumos reguladores, factores y hormonas secretados, como el cortisol en humanos y la corticosterona en roedores.
El cortisol posee propiedades inmunosupresoras. Bajo estrés crónico, el cortisol se produce en exceso; sin embargo, no puede ejercer sus efectos antiinflamatorios. Como resultado, se obstruye la retroalimentación negativa del cortisol en el eje HPA, lo que resulta en hipercortisolemia (Elevación de los niveles de cortisol en la sangre). Este exceso de glucocorticoides inhibe la actividad inmunológica. También aumenta la sensibilidad a las amenazas y el estado de ánimo negativo, deteriora la memoria y otras funciones cognitivas.
La evidencia reciente sugiere una fuerte vía de comunicación bidireccional entre este sistema neuroendocrino y la microbiota intestinal. Se ha identificado que la colonización intestinal por microbios en los primeros años de vida influye en varios aspectos tanto del cerebro como del comportamiento, incluida la respuesta al estrés. Se ha encontrado que el comportamiento de HPA puede afectar la composición de la microbiota intestinal y aumentar la permeabilidad gastrointestinal. Es posible suponer que cualquier cambio en la permeabilidad intestinal y el sistema inmunitario también puede desempeñar un papel importante en las disfunciones neuroendocrinas.
El desequilibrio de la microbiota intestinal puede conducir a la activación del eje HPA. Por lo tanto, restaurar este equilibrio muestra efectos prometedores en la regulación negativa del eje HPA. Varios estudios han demostrado que la suplementación con probióticos logra atenuar significativamente la respuesta del eje HPA al estrés
Respuesta inmune e inflamación
La disbiosis microbiana intestinal a menudo está relacionada con respuestas inmunitarias que incluyen la sobreproducción de citocinas inflamatorias. Los microorganismos en el intestino ayudan a calibrar las respuestas innatas y adaptativasdel sistema inmune, principalmente mediante la producción de pequeñas moléculas que modulan las interacciones huésped-microbiota.
Aunque la barrera epitelial evita que los microorganismos escapen del intestino, los metabolitos que producen pueden atravesar esta barrera y entrar y acumularse en el sistema circulatorio del huésped, donde pueden estimular las células del sistema inmunitario. Además, la microbiota intestinal tiene una fuerte influencia en la población, la migración y la función de varias células inmunitarias.
Varios artículos han demostrado la forma en que los microorganismos intestinales modulan las respuestas inmunitarias tanto innatas como adaptativas en la superficie de la mucosa durante la infección, la inflamación y la autoinmunidad. Las microglías (células del sistema nervioso central que funcionan como elementos del sistema inmunológico, protegiendo al organismo de agresiones externas e internas) son las principales células efectoras de la inmunidad innata del sistema nervioso central.
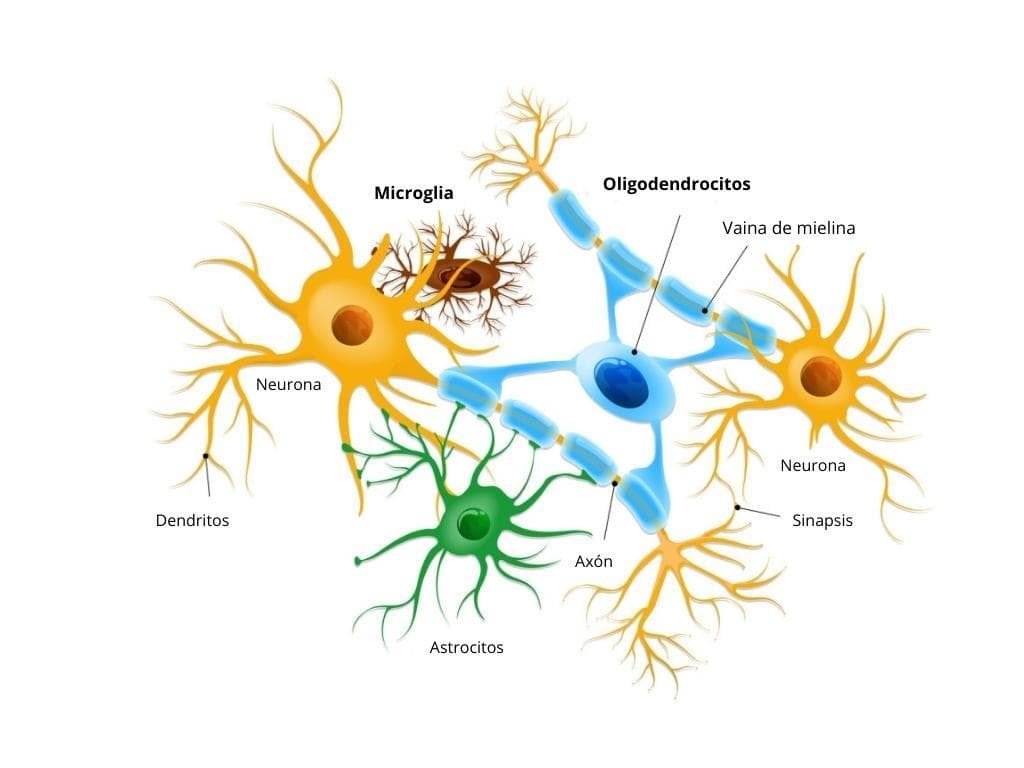
Recientemente se descubrió que la microbiota intestinal juega un papel crucial en la maduración, morfología y función inmunológica de la microglía. Esto se debe a que los ácidos grasos de cadena corta (AGCC) son capaces de interactuar y regular el correcto funcionamiento y desarrollo de la microglía.
Varios artículos publicados recientemente sugieren que los niveles más altos de inflamación aumentan el riesgo de desarrollar trastornos psicológicos. De hecho, se han observado niveles más altos de citocinas inflamatorias en pacientes deprimidos. Además, se ha observado que existe una asociación positiva entre la composición de la microbiota y los niveles séricos de interleucina-1a e interferón-?, que se encuentran positivamente correlacionados con el comportamiento depresivo.
Neurohormonas y neurotransmisores
El microbioma puede producir una variedad de compuestos neuroactivos. Algunos neuroquímicos que se han aislado de las bacterias intestinales son el ácido gamma-aminobutírico (GABA), la noradrenalina, la serotonina, la dopamina y la acetilcolina, que pueden afectar directamente la actividad cerebral. Otros metabolitos bacterianos con funciones neuroactivas incluyen ácidos grasos de cadena larga y corta. Por lo tanto, la capacidad de algunas bacterias dentro del tracto gastrointestinal humano para producir y administrar neurotransmisores y neuromoduladores se ha sugerido como un tratamiento novedoso para enfermedades neuropsiquiátricas.
Si quieres amplian información puedes leer nuestro artículo del blog titulado “El eje microbiota-intestino-cerebro en enfermedades cerebrales agudas y crónicas“
Resumiendo
La depresión y la ansiedad son trastornos mentales con una alta prevalencia a nivel mundial que afectan la calidad de vida de los pacientes e impactan en la economía de regiones enteras. Ya existen tratamientos efectivos para ambos trastornos, pero muchos de ellos tienen efectos secundarios no deseados. Los psicobióticos son una nueva clase de probióticos que poseen propiedades ansiolíticas y antidepresivas en el huésped, acompañadas de cambios en sus estados neurales, emocionales y sistémicos. La evidencia reciente sugiere la participación del eje HPA, la regulación del sistema inmunológico y la inflamación, y la interacción entre los productos de fermentación con el huésped, como los SCFA y los compuestos neuroactivos, como posibles mecanismos de acción detrás del efecto psicobiótico. Una amplia gama de estudios actuales ha demostrado los efectos psicobióticos potenciales que poseen algunas cepas de bacterias y ciertas formulaciones de probióticos contra la depresión y la ansiedad en modelos humanos y murinos (Uso de cepas especiales de ratones para estudiar una enfermedad o afección humana, y la manera de prevenirla y tratarla.).
Bibliografía
- Lou De Santis, G.; Kavvadia, M.; Abd Almajeed Abbaas Alwardat, N.; Bigioni, G.; Zeppieri, C.; Cascapera, S.; De Lorenzo, A. Biomed. Prev. Issues 2017, 2, 111.
- Ait-Belgnaoui, A.; Colom, A.; Braniste, V.; Ramalho, L.; Marrot, A.; Cartier, C.; Houdeau, E.; Theodorou, V.; Tompkins, T. Neurogastroenterol. Motil. 2014, 26, 510–520.
- Andersson, H.; Tullberg, C.; Ahrné, S.; Hamberg, K.; Lazou Ahrén, I.; Molin, G.; Sonesson, M.; Håkansson, Å. Int. J. Microbiol. 2016, 2016, 8469018.
- Schirmer, M.; Smeekens, S.P.; Vlamakis, H.; Jaeger, M.; Oosting, M.; Franzosa, E.A.; ter Horst, R.; Jansen, T.; Jacobs, L.; Bonder, M.J.; Capacity. Cell 2016, 167, 1125–1136.e8.
- Mariano Del Toro-Barbosa, Alejandra Hurtado-Romero, Luis Eduardo Garcia-Amezquita and Tomás García-Cayuela, Nutrients 2020, 12, 3896
- Rea, K.; Dinan, T.G.; Cryan, J.F. Neurobiol. Stress 2016, 4, 23–33.
- Obermeier, B.; Verma, A.; Ransohoff, R.M. The blood–brain barrier. In Handbook of Clinical Neurology; Elsevier: Amsterdam, The Netherlands, 2016; Volume 133, pp. 39–59. ISBN 978-0-444-63432-0.